近日,3344体育会员、省部共建生物催化与酶工程国家重点实验室李珊珊/余希岚团队在Nature子刊(Nature Communications)上以长文形式(Article)发表了题为“Phosphorylation of Jhd2 by the Ras-cAMP-PKA(Tpk2) pathway regulates histone modifications and autophagy”的研究论文。该研究揭示了细胞感知并响应外界营养变化的新机制。湖北大学博士研究生余奇和龚玄云静为该论文共同第一作者,李珊珊教授和余希岚教授为该论文通讯作者,湖北大学为第一单位(图1)。

图1 文章首页
细胞常常处于各种应激压力环境下,这些压力会破坏细胞结构,影响细胞生存。为维持细胞稳态和细胞生长,细胞需要重塑转录组,以适应环境中的营养变化和代谢压力。表观遗传修饰可以动态调控基因表达以响应外界环境改变。早在2015年,李珊珊教授纯化鉴定了糖代谢酶复合物SESAME,它可以直接磷酸化组蛋白,建立了细胞响应葡萄糖变化的表观遗传机制。今年3月份,李珊珊教授与余希岚教授以组蛋白修饰酶SAGA复合物中为研究对象,发现SAGA通过催化自身亚基Ada3的乙酰化,形成SAGA二聚体,进而高效地促进压力应激相关基因的表达,从而提高细胞抵抗环境压力的能力。细胞代谢还可以通过信号分子比如AMPK、mTOR、以及PKA等作为能量感应器来调控基因表达。然而,具体的分子机制尚不完全清楚。
在这项研究中,李珊珊/余希岚团队通过筛选、质谱以及生化技术发现葡萄糖通过激活PKA蛋白激酶家族的催化亚基Tpk2来抑制组蛋白去甲基转移酶Jhd2的酶活性,促进细胞里的组蛋白H3K4三甲基化(H3K4me3),进而调控细胞自噬和衰老。机制上,细胞通过糖代谢产物激活PKA家族催化亚基Tpk2,激活的Tpk2可催化组蛋白去甲基化酶Jhd2的磷酸化。由于Tpk2催化的Jhd2磷酸化位点位于Jhd2的核定位信号序列上,Tpk2催化的Jhd2磷酸化可抑制Jhd2的细胞核定位。Tpk2催化的Jhd2磷酸化还阻止Jhd2结合到染色体上,从而抑制其酶活性。此外,Tpk2催化的Jhd2磷酸化还促进Jhd2被泛素-蛋白酶体降解,进一步提高细胞里的组蛋白H3K4me3。生物信息学分析发现Tpk2催化的Jhd2磷酸化在调控细胞自噬与细胞寿命中起重要作用。在低浓度葡萄糖条件下,Jhd2结合在染色体上抑制自噬基因转录;随着葡萄糖浓度的增加,Tpk2磷酸化Jhd2的活性增强,导致Jhd2被泛素化降解,从而维持细胞的基础自噬水平以及正常的时序性寿命。
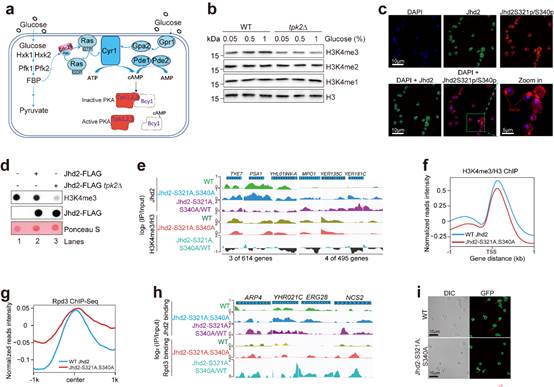
图2 Tpk2通过磷酸化Jhd2调控组蛋白修饰和细胞自噬
李珊珊教授和余希岚教授团队一直从事糖代谢调控衰老与肿瘤发生的表观遗传学研究。自2015年底加盟3344体育会员以来,近5年以湖北大学为第一单位在Nature Metabolism、Nature Structural & Molecular Biology、Nature Communications (2篇)、Nucleic Acids Research (2篇)、Oncogene等国际知名权威期刊上发表20余篇高水平文章,并获得国家自然科学基金面上项目、青年项目、湖北省创新群体、湖北省杰青项目等多项国家级和省部级科研项目的支持。
原文链接:https://doi.org/10.1038/s41467-022-33423-5




